Ключова різниця : І кофактор, і коферменти відіграють надзвичайно важливу роль у метаболічних функціях організму. Кофермент є технічно типом кофактора, де коферменти визначаються як молекули, які вільно пов'язані з ферментом, а кофактори - це ті хімічні сполуки, які зв'язуються з білками.
Іншими сполуками, що впливають на ці реакції, є коферменти і кофактори, які є життєво важливими для надання допомоги ферментам для проведення реакцій. Хоча в реакції обидва функції мають різні властивості і властивості, кофермент є похідною кофактора. Це може бути дуже заплутаним, тому важливо розуміти відмінності між двома хімічними сполуками.
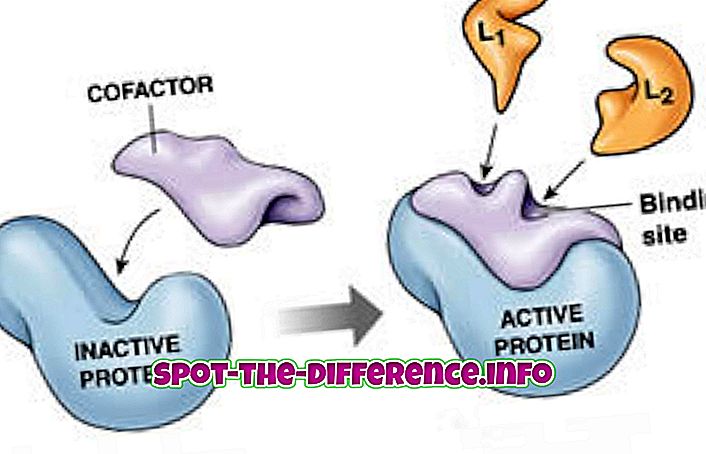
Кофактор являє собою небілкові хімічні сполуки, які щільно або слабо пов'язані з ферментом (білком), з метою підвищення біологічної активності сполуки. Вона надзвичайно важлива і використовується в якості каталізатора в реакції. Вона також називається "хелперною молекулою" через її біохімічні перетворення в реакціях. Є буксирні типи кофакторів:
- Коферменти
- Протетичні групи
З іншого боку, коферменти визначаються як невеликі, органічні, небілкові молекули, такі як вітаміни, які несуть хімічні групи між ферментами. Хоча, він не вважається частиною ферментної структури, на коферменти впливають ферменти для реакції. Він також відомий як ко-субстрати.

З іншого боку, кофактори необхідні і необхідні для збільшення і аналізу швидкості реакції, тобто, наскільки швидко каталізатор буде діяти для завершення реакції. Багато разів, кофактори і коферменти мають подібні функції, такі як регулювання, контроль і регулювання темпів цих хімічних реакцій і їх вплив на організм. Проте, відмінності між ними наведені в таблиці нижче.
Порівняння між кофактором і коферментом:
Кофактор | Кофермент | |
Визначення | Це небілкові хімічні сполуки, які щільно або слабо пов'язані з ферментом (білком). | Вона визначається як невеликі, органічні, небілкові молекули, які несуть хімічні групи між ферментами. |
Характеристики | Це неорганічні речовини. | Це органічні речовини. |
Функція | Він допомагає в біологічних перетвореннях. | Вона допомагає або допомагає функції ферменту. |
Тип | Це хімічні сполуки. | Це хімічні молекули. |
Зв'язаний | Він щільно прив'язаний до ферменту. | Вона вільно прив'язана до ферменту. |
Дія | Вони діють на каталізатор для збільшення швидкості реакції. | Вони діють як переносить ферменти. |
Приклад | Металеві іони, такі як Zn ++, K + і Mg ++ і т.д. | Вітаміни, біотин, кофермент А та ін |